Mikrofluidik-System verbessert Superauflösungsmikroskopie
Ein internationales Forscherteam verbessert mit Hilfe eines Mikrofluidik-Systems die Bildgebung vom komplexen Inneren der Zellen der Superauflösungsmikroskopie.
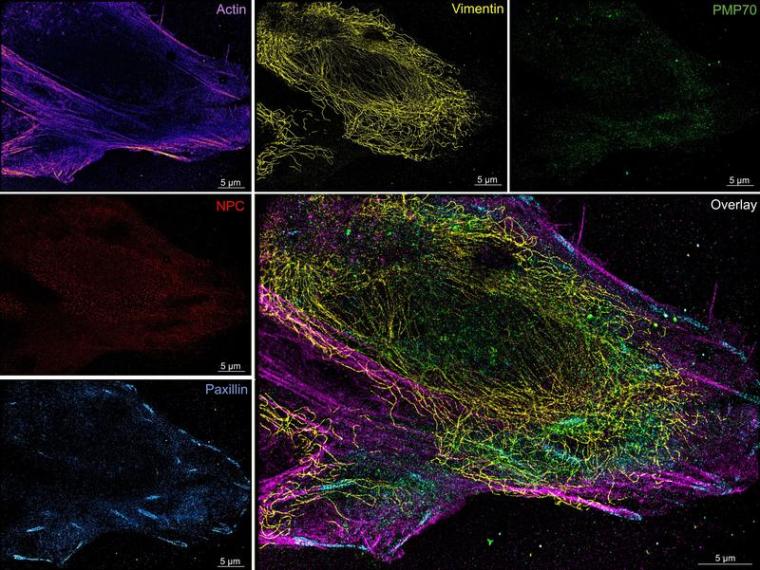
Wie sind Zellen organisiert? Und wie arbeiten ihre molekularen Bestandteile zusammen? Das zu verstehen, ist ein zentrales Ziel moderner Life Sciences. Forscher müssen dabei viele Strukturen in einer Zelle gleichzeitig betrachten, um zu erkennen, wie sie angeordnet sind und interagieren. Das gelingt nur mit einem Bildgebungsverfahren, das zelluläre Details weit über die Grenzen herkömmlicher Lichtmikroskope hinaus sichtbar macht: die multiplexe Superauflösungsmikroskopie. Die Technik ist allerdings anspruchsvoll, für empfindliche Proben ungeeignet und störungsanfällig.
Wiederholbare Ergebnisse damit zu erzeugen, ist zudem schwierig. Ein internationales Forscherteam hat nun ein Mikrofluidik-System entwickelt, das diese hochaufgelöste Mikroskopie einfacher, reproduzierbarer und mehr Forschern zugänglich macht. Die Arbeit wurde von Forschern der Universität und der Universitätsmedizin Göttingen (UMG) im Rahmen des Göttinger Exzellenzclusters „Multiscale Bioimaging: From Molecular Machines to Networks of Excitable Cells” (MBExC) geleitet und in der Fachzeitschrift ACS Nano veröffentlicht.
Lange Bildgebungszyklen
Das neue Mikrofluidik-System injiziert und entfernt Lösungen präzise aus der Kammer, in der sich die Zellprobe befindet. Damit müssen Forscher dies nicht mehr mit einer Pipette und nach strengen Vorgaben selbst erledigen. „Mit dem von uns entwickelten System können wir über lange Bildgebungszyklen hinweg eine hohe Bildqualität aufrechterhalten“, erklärt Dr. Samrat Basak, der als Biophysiker an der Universität Göttingen an der Studie mitgewirkt hat und inzwischen an der LMU München arbeitet. „Durch die gleichbleibenden Bedingungen während der verschiedenen Markierungs- und Waschschritte macht das Mikrofluidik-System es möglich, Informationen von verschiedenen markierten Biomolekülen genau zuzuordnen. So lassen sich Proteine, spezialisierte Strukturen und komplexe Interaktionen innerhalb der Zelle abbilden.“
Manuell oder automatisiert
Die Forscher haben die Technik an menschlichen Krebszellen demonstriert. Sie zeigten damit, wie Proteinfilamente in diesen Zellen organisiert sind. Sie wandten die Methode zudem auf Muskelzellen aus den Herzkammern einer Maus an. „Die empfindlichen, spezialisierten Muskelzellen des Herzens sind besonders schwer abzubilden“, erklärt Kim-Chi Vu von der UMG und MBExC. „Das Mikrofluidik-System war unerlässlich, um die Bildgebung durchzuführen, ohne die Zellen zu verformen oder von der Oberfläche zu lösen.“
Das Mikrofluidik-System kann sowohl manuell als auch automatisiert betrieben werden. Es ist zudem mit einer Vielzahl von Bildgebungsverfahren kompatibel. „Unser Ziel war es, ein System zu entwickeln, das kosteneffizient sowie anpassungsfähig ist und somit passend zu den spezifischen Anforderungen an die Bildgebung komplexer biologischer Systeme gestaltet werden kann“, erklärt Dr. Roman Tsukanov aus der Multiskalen-Biologie der Universität Göttingen, der die Studie geleitet hat. „Durch die Automatisierung des Flüssigkeitsaustauschs haben wir eine wichtige Quelle für Abweichungen beseitigt und komplexe Bildgebungsprotokolle wesentlich benutzerfreundlicher gemacht.“ Prof. Dr. Jörg Enderlein aus der Biophysik der Universität Göttingen sowie vom Exzellenzcluster MBExC fügt hinzu: „Dieser Ansatz wird dazu beitragen, die multiplexe Superauflösungsbildgebung zu standardisieren und allgemein zugänglich zu machen. Das kommt sowohl der Forschung als auch medizinischen Anwendungen zugute.“