Nährstoff-Timing beeinflusst Genaktivität im Fettgewebe
Ob wir morgens eher Kohlenhydrate oder Fette essen, könnte mitbestimmen, wie unser Stoffwechsel arbeitet.

Prof. Olga Ramich vom Deutschen Institut für Ernährungsforschung Potsdam-Rehbrücke (DIfE) und der Charité – Universitätsmedizin Berlin hat gemeinsam mit ihrem Team nun erstmals am Menschen gezeigt, dass die zeitliche Verteilung der Aufnahme von Kohlenhydraten und Fetten die Aktivität von mehr als tausend Genen im Fettgewebe über den Tag hinweg verändert – darunter Gene, die den Zucker- und Fettstoffwechsel sowie Entzündungsprozesse steuern. Die Ergebnisse wurden im Fachjournal Food Research International veröffentlicht.
Der menschliche Stoffwechsel wird von der inneren Uhr gesteuert und folgt zirkadianen Rhythmen. Viele Prozesse, wie zum Beispiel die Zuckeraufnahme, Fettverbrennung oder Hormonfreisetzung, oszillieren im Tagesverlauf, d. h., sie schwanken und weisen charakteristische 24-stündige Rhythmen auf. Wenn Nährstoffe außerhalb der für die inneren Rhythmen optimalen Zeitfenster konsumiert werden, könnte das langfristig Stoffwechselstörungen begünstigen. Das Forschungsgebiet der Chrononutrition untersucht die zugrunde liegenden molekularen Mechanismen, um Essenszeiten optimal zu timen, die Stoffwechselgesundheit zu steigern und chronische Erkrankungen zu verhindern.
Fette zum Frühstück oder zum Abendbrot?
Prof. Olga Ramich, Leiterin der Abteilung Molekularer Stoffwechsel und Präzisionsernährung am DIfE, und ihr Team untersuchten erstmalig an Menschen, ob der Zeitpunkt der Aufnahme von Kohlenhydraten und Fetten die tageszeitliche Genexpression im Unterhautfettgewebe unabhängig von der Kalorienaufnahme verändert. Dafür nutzten sie Daten aus einer kontrollierten Ernährungsstudie im Crossover-Design, an der 29 übergewichtige Männer ohne Diabetes teilnahmen. Die Probanden folgten jeweils vier Wochen lang zwei unterschiedlichen Ernährungsplänen, die hinsichtlich ihrer Kalorienmenge identisch (isokalorisch) waren. Während einer Ernährungsintervention nahmen sie morgens viele Kohlenhydrate und abends viel Fett auf, bei der zweiten Intervention war es genau anders herum. Auf Grund des verwendeten Crossover-Ansatzes erhielten alle Teilnehmer beide Interventionen, sodass individuelle Unterschiede in der Stoffwechselantwort besser isoliert werden konnten.
Das Studienteam entnahm den Teilnehmern vor und nach jeder Ernährungsintervention zu verschiedenen Tageszeiten jeweils drei Proben aus dem Unterhautfettgewebe. In Kooperation mit Prof. Achim Kramer, Leiter des Arbeitsbereichs Chronobiologie an der Klinik für Anästhesiologie und Intensivmedizin der Charité, wurde daraufhin das Transkriptom analysiert, das ein dynamisches Abbild der Genaktivität darstellt.
Deutliche Unterschiede im Fettgewebe
Erstmals charakterisierten Ramich und ihr Team die Genrhythmen im Unterhautfettgewebe und konnten feststellen, dass die tageszeitliche Nährstoffverteilung das oszillierende und nicht-oszillierende Transkriptom veränderte.
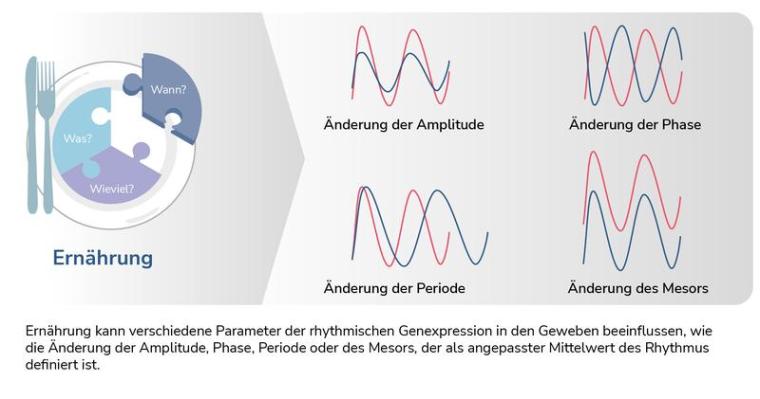
Die Analysen zeigten, dass 1.386 Gene im untersuchten Fettgewebe tageszeitlichen Oszillationen unterliegen. Viele dieser Gene sind mit dem Glukose- und Fettstoffwechsel oder mit Entzündungsprozessen assoziiert. Die Wissenschaftler*innen stellten fest, dass der Zeitpunkt der Makronährstoffaufnahme die tageszeitliche Genexpression von fast einem Drittel der oszillierenden Gene im Fettgewebe beeinflusste. Manche Gene wiesen veränderte Rhythmenparameter auf, andere stellten die Oszillation ein oder, umgekehrt, nicht-oszillierende Gene wurden zu oszillierenden.
Der Verzehr von fettreicher Kost am Morgen und kohlenhydratreicher Nahrung am Abend führte zu einer Verbesserung der Marker für die Insulinsensitivität im untersuchten Fettgewebe. Eine Verschiebung der Fettaufnahme in den Abend hingegen erhöhte die Aktivität von Entzündungsgenen. Das könnte ein Hinweis auf einen frühen proinflammatorischen Zustand im Fettgewebe sein, welcher als Risikofaktor für die Entstehung metabolischer Erkrankungen wie Adipositas und Typ-2-Diabetes gilt.
Neuer Ansatz für Prävention
„Unsere Ergebnisse bestätigen erste Erkenntnisse, dass die Verschiebung der Makronährstoffverteilung über den Tag die metabolischen Prozesse im Fettgewebe messbar beeinflusst“, sagt Ramich. „Späte, fettreiche Mahlzeiten könnten vielleicht ungünstige molekulare Prozesse anstoßen, die möglicherweise langfristig Entzündungen und Stoffwechselprobleme fördern.“
Die Forschenden sehen in ihren Ergebnissen neue Ansatzpunkte für die Prävention von Übergewicht und Typ-2-Diabetes. „Neben Kalorienmenge und Nährstoffzusammensetzung könnte zukünftig auch das Mahlzeiten-Timing ein wichtiger Bestandteil personalisierter Ernährungsempfehlungen sein“, erklärt Ramich.
Allerdings betonen die Wissenschaftler*innen, dass größere und langfristige Interventionsstudien nötig sind, um gesundheitliche Auswirkungen oder gar Empfehlungen für unterschiedliche Bevölkerungsgruppen, wie z. B. Frauen und/oder Menschen mit Diabetes, abzuleiten. Auch mechanistische Studien in Zellkultur- oder tierexperimentellen Modellen könnten helfen, den Zusammenhang zwischen zirkadianen Änderungen im Fettgewebe und dem Gesamtstoffwechsel genauer zu untersuchen.
Anbieter