
Welche Anforderungen gelten für künftige KI-Medizinprodukte?
Die KI-VO birgt Innovationschancen für kontinuierlich lernende KI-Medizinprodukte – aber vor allem Start-Ups und KMU stehen vor vielfältigen Herausforderungen.

Die KI-VO birgt Innovationschancen für kontinuierlich lernende KI-Medizinprodukte – aber vor allem Start-Ups und KMU stehen vor vielfältigen Herausforderungen.

Medizinischer Co-Pilot: Erstes KI-gestütztes Medizinprodukt ist zur Unterstützung klinischer Entscheidungen zugelassen.

Die Jury des Eugen Münch-Preises für innovative Gesundheitsversorgung hat die Gewinner für das Jahr 2024 ausgewählt.

Die BGW bietet ein umfangreiches Angebot an Weiterbildung, das Führungskräfte und Teams fit für den Arbeitsalltag macht.

Der Bundesverband Medizintechnologie (BVMed) weist zum „Internationalen Tag der Pflegenden“ am 12. Mai darauf hin, dass moderne Medizintechnologien einen wertvollen Beitrag zur Unterstützung und Entlastung der Pflege leisten können.

TÜV SÜD hat als eine der wenigen Benannten Stellen noch Kapazitäten für Konformitätsbewertungsverfahren von Medizinprodukten mit der Medical Device Regulation (MDR) und der In Vitro Diagnostic Regulation (IVDR).

Hersteller und Anwender von Medizinprodukten fordern längst überfällige Möglichkeit zur Nutzung elektronischer Gebrauchsanweisungen.

Gesundheits-Apps umfassen eine Vielzahl von Produkten unterschiedlicher Qualität. Serviceorientierte und medizinische Anwendungen unterstützen bei Therapie und Befund.

Der Bundesverband Medizintechnologie (BVMed) klärt mit einem Informationsblatt über Handlungsbedarfe und Verfahrenspflichten auf, die sich für Medizinprodukte-Unternehmen aus dem neuen Hinweisgeber-Schutzgesetz (HinSchG) ergeben.

LLM-basierte generative Chat-Tools wie ChatGPT oder MedPaLM von Google haben großes medizinisches Potenzial, ihre unregulierte Verwendung im Gesundheitswesen birgt jedoch inhärente Risiken.

Zusammen mit einer großen Gruppe führender europäischer Verbände aus dem Bereich der Kindermedizin hat sich die Stiftung Kindergesundheit in einem offenen Brief an EU-Gesundheitskommissarin Stella Kyriakides gewandt. Darin fordern die Organisationen dazu auf, den Zugang von Kindern und Patient*innen mit seltenen Krankheiten zu lebenswichtigen Medizinprodukten sicherzustellen.

Weltweit ist eine Sensibilisierung der Regulierer für Cybersecurity zu erkennen. Doch wer kümmert sich um die Cybersicherheit für Medizinprodukte?
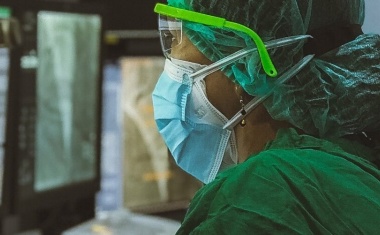
Der TÜV-Verband wird Partner des „EU TEF-Health Projekts“.

Richtlinie VDI 5707 Blatt 1 ist Grundlage für evidenzbasierte Wiederholungsprüfungen an aktiven Medizinprodukten.

Der Bundesverband Medizintechnologie (BVMed) baut ein wissenschaftliches Institut auf, das sich unter anderem der Versorgungs- und Gesundheitssystemforschung sowie Fragen der Methoden- und Nutzenbewertung von Medizinprodukten widmen wird.

Unternehmen im Gesundheitsmarkt stehen heute vor besonderen Herausforderungen. Welche Möglichkeiten gibt es bei Liquiditätsengpässen? Wie sichert die Politik die finanzielle Unterstützung für Einrichtungen des Gesundheitswesens? Worauf müssen sich Hersteller von Medizinprodukten einstellen?


Unruhe breitet sich zurzeit im Markt für Medizinprodukte aus. Eine Konsolidierungswelle erfasst selbst die ganz großen Unternehmen in der Branche.

Führender Hersteller medizinischer Betten gestaltet jetzt die Zukunft.

500 Gäste feierten ersten Medizin Messe Kongress im Ruhrgebiet.
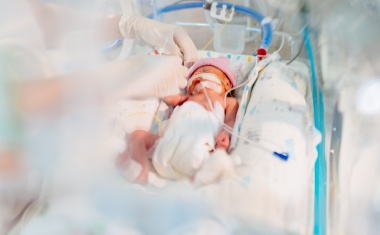
Warum sind CE-gekennzeichnete Medizinprodukte wichtig für den Klinikalltag?
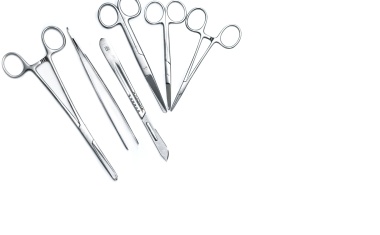
Die sichere Aufbereitung von Medizinprodukten ist sehr aufwendig, aber unverzichtbar.

Fraunhofer IWKS und IRED Institut starten eine Kooperationsplattform, um das Recycling medizinischer Produkte voranzutreiben.


Speziell dort, wo Lebensmittel verarbeitet und Medizininstrumente behandelt werden, ist absolute Sauberkeit unerlässlich.






























